・これから医薬部外品を輸入して、販売したい
・取引先から医薬部外品を保管してほしいと頼まれている
・許可取得したいけど、どうすればいいか分からない・・・
CJ Link Services行政書士法人によくいただくご相談の内容です。
当事務所では、医薬部外品に関する許可の取得サポートをしています。
この許可を取得するためには、許可基準をクリアする必要があります。
当事務所では、現状での許可取得の可否判断から、どうすれば許可を取得できるのか等のコンサルティング、
書類作成、申請代行まで一括したサポートが可能です。
これまで多くのサポート実績を積んできた当事務所にお任せください!
<目次>
(医薬部外品製造販売業)
(医薬部外品製造業)
サービス一覧・報酬表
医薬部外品に関する許可のサービスは次の通りです。
報酬額についてもお伝えしますので、まずはこちらをご確認ください!

医薬部外品とは
医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(略称:医薬品医療機器等法)において、
下記のように定義されています。
「医薬部外品」とは、次に掲げる物であって人体に対する作用が緩和なものをいう。
一 次のイからハまでに掲げる目的のために使用される物(これらの使用目的の他に、
併せて医薬品に規定する目的のために使用されるものを除く。)であって機械器具等でないもの
イ 吐きけその他の不快感又は口臭若しくは体臭の防止
ロ あせも、ただれ等の防止
ハ 脱毛の防止、育毛又は除毛
二 人又は動物の保健のためにするねずみ、はえ、蚊、のみその他これらに類する生物の防除の目的のために
使用される物これらの使用目的の他に、併せて医薬品に規定する目的のために使用されるものを除く。)
であって機械器具等でないもの
三 医薬品に規定する目的のために使用される物のうち、厚生労働大臣が指定するもの
つまり、医薬部外品とは、「医薬品」に定める治療を目的にしたものではなく、「防止・衛生」を目的にしたものとなります。
「三 厚生労働大臣が指定するもの」については、平成11年3月に規制緩和により
医薬品から医薬部外品に移行された製品(新指定医薬部外品)や、平成16年7月に医薬品から移行された
整腸薬や殺菌消毒薬などの製品(新範囲医薬部外品)が含まれています。
厚生労働大臣が指定する医薬部外品をまとめた表です。【H21.2.6 厚告第25号】
|
(1) |
胃の不快感を改善することが目的とされている物 |
新指定 |
|
(2) |
いびき防止薬 |
新範囲 |
|
(3) |
衛生上の用に供されることが目的とされている綿類 (紙綿類を含む。) |
|
|
(4) |
カルシウムを主たる有効成分とする保健薬 ((19)に掲げるものを除く。) |
新範囲 |
|
(5) |
含嗽薬(がんそうやく) |
新範囲 |
|
(6) |
健胃薬((1)及び(27)に掲げるものを除く。) |
新範囲 |
|
(7) |
口腔咽喉薬((20)に掲げるものを除く。) |
新範囲 |
|
(8) |
コンタクトレンズ装着薬 |
新範囲 |
|
(9) |
殺菌消毒薬((15)に掲げるものを除く。) |
新範囲 |
|
(10) |
しもやけ・あかぎれ用薬((24)に掲げるものを除く。) |
新範囲 |
|
(11) |
瀉下薬 |
新範囲 |
|
(12) |
消化薬((27)に掲げるものを除く。) |
新範囲 |
|
(13) |
滋養強壮、虚弱体質の改善及び栄養補給が目的とされている物 |
新指定 |
|
(14) |
生薬を主たる有効成分とする保健薬 |
新範囲 |
|
(15) |
すり傷、切り傷、さし傷、かき傷、靴ずれ、創傷面等の消毒又は保護に使用されることが目的とされている物 |
新指定 |
|
(16) |
整腸薬((27)に掲げるものを除く。) |
新範囲 |
|
(17) |
染毛剤 |
|
|
(18) |
ソフトコンタクトレンズ用消毒剤 |
|
|
(19) |
肉体疲労時、中高年期等のビタミン又はカルシウムの補給が目的とされている物 |
新指定 |
|
(20) |
のどの不快感を改善することが目的とされている物 |
新指定 |
|
(21) |
パーマネント・ウェーブ用剤 |
|
|
(22) |
鼻づまり改善薬(外用剤に限る。) |
新範囲 |
|
(23) |
ビタミンを含有する保健薬((13)及び(19)に掲げるものを除く。) |
新範囲 |
|
(24) |
ひび、あかぎれ、あせも、ただれ、うおのめ、たこ、手足のあれ、かさつき等を改善することが目的とされている物 |
新指定 |
|
(25) |
医薬品医療機器等法第二条第三項(「化粧品」とはを定義する項)に規定する使用目的のほかに、にきび、肌荒れ、かぶれ、しもやけ等の防止又は皮膚若しくは口腔の殺菌消毒に使用されることも併せて目的とされている物 |
|
|
(26) |
浴用剤 |
|
|
(27) |
(6)、(12)又は(16)に掲げる物のうち、いずれか二以上に該当するもの |
新範囲 |
医薬部外品の効能・効果の範囲
医薬部外品の効能効果の範囲については、概ね以下の表の通りであるとされています。
【薬生監麻発0929 第5 号】
〇医薬部外品の効能・効果の範囲
|
医薬部外品の種類 |
使用目的の範囲と原則的な剤型 |
効能又は効果の範囲 |
|
|
使用目的 |
主な剤型 |
効能又は効果 |
|
|
1.口内清涼剤 |
吐き気その他の不快感の防止。 |
トローチ、液体 |
口臭、気分不快。 |
|
2.腋臭防止剤 |
体臭の防止を目的とする外用剤。 |
液体、軟膏、エアゾール |
わきが(腋臭) 、皮膚汗臭、制汗。 |
|
3.てんか粉類 |
あせも、ただれ等の防止を目的とする外用剤。 |
外用散布剤 |
あせも、おしめ(おむつ)、かぶれ、ただれ、股ずれ、かみそりまけ。 |
|
4.育毛剤(養毛剤) |
脱毛の防止及び育毛を目的とする外用剤。 |
液体、エアゾール |
育毛、薄毛、かゆみ、脱毛の予防、毛生促進、発毛促進、ふけ、病後・産後の脱毛、養毛。 |
|
5.除毛剤 |
除毛を目的とする外用剤。 |
軟膏剤、エアゾール剤 |
除毛。 |
|
6.染毛剤 (脱色剤、脱染剤) |
毛髪の染色、脱色または脱染を目的とする外用剤(毛髪を単に物理的に染色するもの(化粧品)は除く。) |
粉末状、打型状、エアゾール、液状又はクリーム状 |
染毛、脱色、脱染のうち、目的に応じて設定。 |
|
7.パーマネント・ ウェーブ剤 |
毛髪のウェーブ等を目的とする頭髪用の外用剤。 (手足等の体毛及び眉毛・まつ毛は除く。) |
第1剤にあっては液状、ねり状、クリーム状、エアゾール剤等とし、第2剤にあっては、粉末状、打型状、液状、ねり状、クリーム状、エアゾール等 |
毛髪にウェーブをもたせ、保つ。くせ毛、ちぢれ毛、またはウェーブ毛髪をのばし、保つ。 |
|
8.衛生綿類 |
衛生上の用に供されることが目的とされている綿類(紙綿類を含む。) |
綿類、ガーゼ |
生理処理用品については生理処理用、清浄用綿類については乳児の皮膚・口腔の清浄・清拭または授乳時の乳首・乳房の清浄・清拭、目、局部、肛門の清浄・清拭 |
|
9.浴用剤 |
原則としてその使用法が浴槽中に投入して用いられる外用剤。(浴用石けんは浴用剤には該当しない。) |
粉末状、粒状、打型状、カプセル、液状等 |
あせも、荒れ性、うちみ、肩のこり、くじき、神経痛、湿疹、しもやけ、痔、冷え症、腰痛、リウマチ、疲労回復、ひび、あかぎれ、産前産後の冷え症、にきび。 |
|
10.薬用化粧品 (薬用石けんを含む) |
化粧品としての使用目的を合わせて有する化粧品類似の剤型の外用剤。 |
液状、クリーム状、ゼリー状、固型状、エアゾール |
(別掲)※下記「薬用化粧品の効能・効果の範囲」参照 |
|
11.薬用歯みがき類 |
化粧品としての使用目的を有する通常の歯みがきと類似の剤型の外用剤。 |
ペースト状、液状、粉末状、固型状、潤製状 |
歯を白くする、口中を浄化する、口中を爽快にする、歯周炎(歯槽膿漏)の予防、歯肉炎の予防、歯石の沈着を防ぐ、むし歯を防ぐ、むし歯の発生及び進行の予防、口臭の防止、タバコのヤニ除去 |
|
12.忌避剤 |
はえ、蚊、のみ等の忌避を目的とする外用剤。 |
液状、チック様、クリーム状の剤型、エアゾール剤 |
蚊成虫、ブヨ、サシバエ、ノミ、イエダニ、トコジラミ(ナンキンムシ)等の忌避 |
|
13.殺虫剤 |
はえ、蚊、のみ等の駆除または防止の目的を有するものである。 |
マット、線香、粉剤、液剤、エアゾール剤、ペースト状の剤型 |
殺虫。 |
|
14.殺そ剤 |
ねずみの駆除または防止の目的を有するもの。 |
ねずみの駆除。 |
|
|
15.ソフトコンタクトレンズ用消毒剤 |
ソフトコンタクトレンズの消毒を目的とするもの。 |
液状 |
ソフトコンタクトレンズの消毒。 |
〇薬用化粧品の効能・効果の範囲
|
種 類 |
効能・効果 |
|
1.シャンプー |
ふけ・かゆみを防ぐ。 毛髪・頭皮の汗臭を防ぐ。 毛髪・頭皮を清浄にする。 毛髪・頭皮をすこやかに保つ。 毛髪をしなやかにする。 |
|
2.リンス |
ふけ・かゆみを防ぐ。 毛髪・頭皮の汗臭を防ぐ。 毛髪の水分・脂肪を補い保つ。 裂毛・切毛・枝毛を防ぐ。 毛髪・頭皮をすこやかに保つ。 毛髪をしなやかにする。 |
|
3.化粧水 |
肌あれ。あれ性。 あせも・しもやけ・ひび・あかぎれ・にきびを防ぐ。 油性肌。 かみそりまけを防ぐ。 日やけによるしみ・そばかすを防ぐ。 日やけ・雪やけ後のほてりを防ぐ。 肌をひきしめる。肌を清浄にする。肌を整える。 皮膚をすこやかに保つ。皮膚にうるおいを与える。 |
|
4.クリーム・乳液・ハンドクリーム・化粧用油 |
肌あれ。あれ性。 あせも・しもやけ・ひび・あかぎれ・にきびを防ぐ。 油性肌。 かみそりまけを防ぐ。 日やけによるしみ・そばかすを防ぐ。 日やけ・雪やけ後のほてりを防ぐ。 肌をひきしめる。肌を清浄にする。肌を整える。 皮膚をすこやかに保つ。皮膚にうるおいを与える。 皮膚を保護する。皮膚の乾燥を防ぐ。 |
|
5.ひげそり用剤 |
かみそりまけを防ぐ。 皮膚を保護し、ひげをそりやすくする。 |
|
6.日やけ止め剤 |
日やけ・雪やけによる肌あれを防ぐ。 日やけ・雪やけを防ぐ。 日やけによるしみ・そばかすを防ぐ。 皮膚を保護する。 |
|
7.パック |
肌あれ。あれ性。 にきびを防ぐ。 油性肌。 日やけによるしみ・そばかすを防ぐ。 日やけ・雪やけ後のほてり。 肌をなめらかにする。 皮膚を清浄にする。 |
|
8.薬用石けん (洗顔料を含む) |
< 殺菌剤主剤のもの> 皮膚の清浄・殺菌・消毒。 体臭・汗臭及びにきびを防ぐ。 < 消炎剤主剤のもの> 皮膚の清浄、にきび・かみそりまけ及び肌あれを防ぐ。 |
〇新指定医薬部外品の効能・効果の範囲
|
製品群 |
剤型 |
効能・効果 |
|
のど清涼剤 |
トローチ剤 ドロップ剤 |
たん,のどの炎症による声がれ・のどのあれ・のどの不快感・のどの痛み・のどのはれ |
|
健胃清涼剤 |
カプセル剤 顆粒剤 丸剤・散剤 舐剤・錠剤 内用液剤 |
食べ過ぎ,飲み過ぎによる胃部不快感,はきけ(むかつき,胃のむかつき,二日酔・悪酔いのむかつき,嘔気,悪心) |
|
外皮消毒剤 |
外用液剤 軟膏剤 |
すり傷,切り傷,さし傷,かき傷,靴ずれ,創傷面の洗浄・消毒手指・皮膚の洗浄・消毒 |
|
きず消毒保護剤 |
絆創膏類 外用液剤 |
すり傷,切り傷,さし傷,かき傷,靴ずれ,創傷面の消毒・保護(被覆) |
|
ひび・あかぎれ用剤 (クロルヘキシジン主剤) |
軟膏剤 |
ひび・あかぎれ・すり傷・靴ずれ |
|
ひび・あかぎれ用剤 (メントール・カンフル主剤) |
ひび・しもやけ・あかぎれ |
|
|
ひび・あかぎれ用剤 (ビタミンAE 主剤) |
ひび・しもやけ・あかぎれ・手足のあれの緩和 |
|
|
あせも・ただれ用剤 |
外用液剤 軟膏剤 |
あせも・ただれの緩和・防止 |
|
うおのめ・たこ用剤 |
絆創膏 |
うおのめ・たこ |
|
かさつき・あれ用剤 |
軟膏剤 |
手足のかさつき・あれの緩和 |
|
ビタミンC剤 |
カプセル剤 顆粒剤 丸剤・散剤 舐剤・錠剤 ゼリー状ドロップ内用液剤 |
肉体疲労時,妊娠・授乳期,病中病後の体力低下時又は中高年期のビタミンC の補給 |
|
ビタミンE剤 |
中高年期のビタミンE の補給 |
|
|
ビタミンEC剤 |
肉体疲労時,病中病後の体力低下時又は中高年期のビタミンEC の補給 |
|
|
ビタミン含有保健剤 |
カプセル剤 顆粒剤 丸剤・散剤 錠剤 内用液剤 |
滋養強壮,虚弱体質,肉体疲労・病中病後(又は病後の体力低下)・食欲不振(又は胃腸障害)・栄養障害・発熱性消耗性疾患・妊娠授乳期(又は産前産後)(ビタミンA,D を含まないもの)などの場合の栄養補給 |
|
カルシウム剤 |
カプセル剤 顆粒剤 散剤・錠剤 内用液剤 |
妊娠授乳期・発育期・中高年期のカルシウムの補給 |
医薬部外品製造販売業・医薬部外品製造業とは
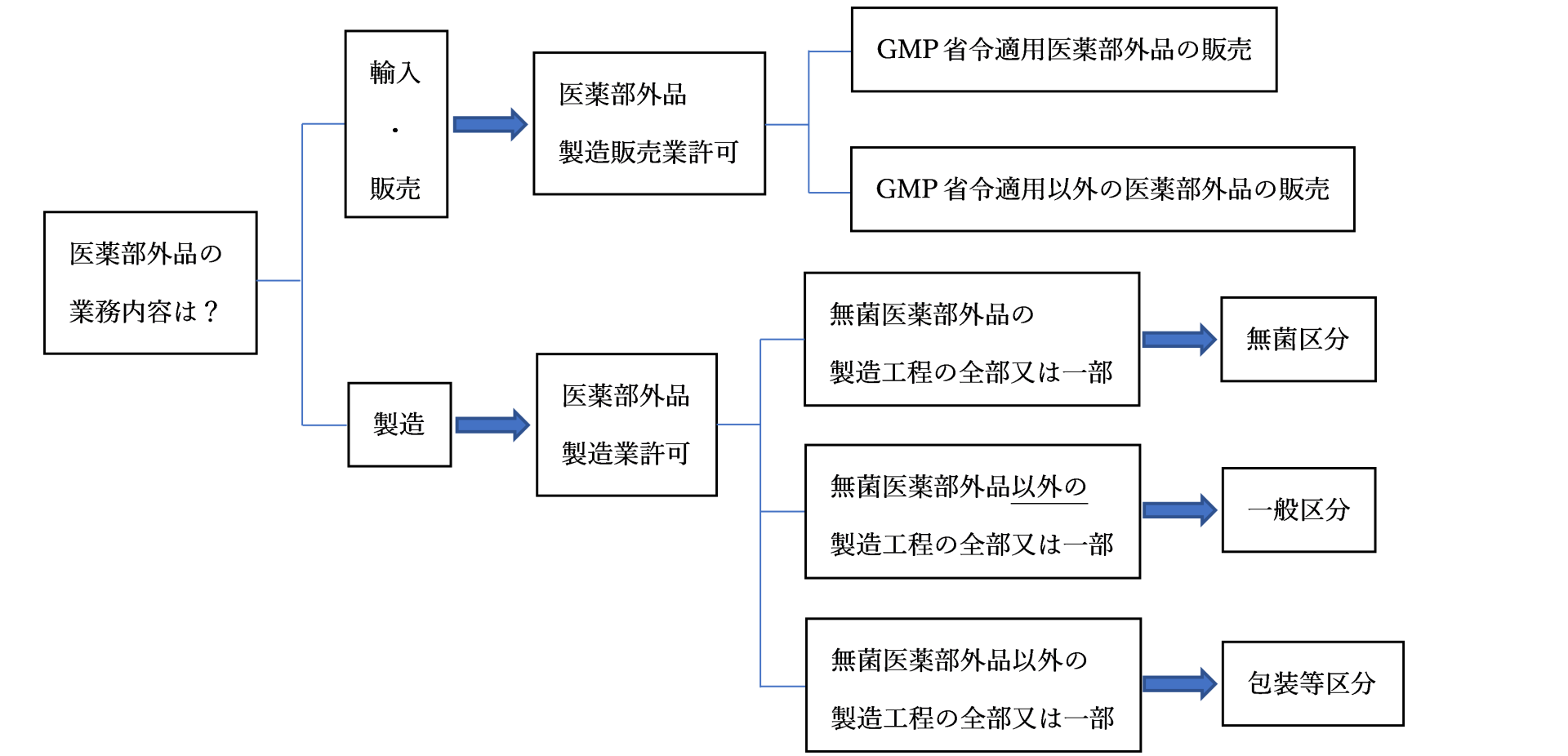
医薬部外品の許可には、
医薬部外品製造販売業許可と医薬部外品製造業許可に分かれており、
GMP適用の医薬部外品か否かによっても、製造販売業許可・製造業の種類が異なります。
また、製造業許可は、行う製造工程の種類によって、一般区分・無菌区分・包装等区分に分類されています。
★製造販売とは・・・
薬機法で定める「製造販売」とは、その製造等(他に委託して製造する場合を含み、
他から委託を受けて製造する場合を含まない。)をし、又は輸入した医薬部外品を販売し、賃貸し、又は授与することを言います。
★製造販売業とは・・・
製造販売業者とは、市場に出荷・上市する製品の品質や有効性、安全性などの最終的な責任を負う者を指します。
つまり、「製品についての流通責任を負う者」です。また、品質だけでなく、安全性についても
積極的に収集・分析・評価を行い、必要な措置を逐次講ずることが求められます。
★製造とは・・・
製造とは、一般的に製品の製造の事を指しますが、薬機法上では、製品の包装・表示・保管などの
工程のみを行う場合でも製造であるとされています。
無菌医薬部外品以外の製造工程のうち全行程を行う場合は製造業許可(一般区分)、
無菌医薬部外品の製造工程のうち全行程を行う場合は製造業許可(無菌区分)、
包装・表示・保管のみを行う場合は製造業許可(包装等区分)の許可が必要となります。
★製造業者とは・・・
製造業者とは、製造販売業者の既承認品目の製造に係る委託を受けることで、自ら承認を得ることなく、
当該品目の製造を行うことが可能な者を指します。製造した製品は、製造販売業者又は製造業者にのみ
販売・賃貸・授与することができ、製造業者として、製造した医薬部外品を市場に出荷・上市することはできません。
医薬部外品製造販売業
クリアすべき許可要件は何?
医薬部外品製造販売業許可を取得するためには必要な要件は、下記の通りです。
①申請者が欠格要件に該当しないこと
②適正な業務運営を確保するための手順書(GQP、GMP)の整備
③責任者の設置
①申請者が欠格要件に該当しないこと
申請者が、下記のいずれかに該当するときは、許可を与えないことができる。
【薬機法第12条の2第3項】
イ 第75条第1項の規定により許可を取り消され、取消しの日から3年を経過していない者
ロ 第75条の2第1項の規定により登録を取り消され、取消しの日から3年を経過していない者
ハ 禁錮以上の刑に処せられ、その執行を終わり、又は執行を受けることがなくなった後、3年を経過していない者
ニ イからハまでに該当する者を除くほか、この法律、麻薬及び向精神薬取締法、
毒物及び劇物取締法(昭和25年法律第303号)その他薬事に関する法令で政令で定めるもの
又はこれに基づく処分に違反し、その違反行為があつた日から2年を経過していない者
ホ 成年被後見人又は麻薬、大麻、あへん若しくは覚醒剤の中毒者
ヘ 心身の障害により薬局開設者の業務を適正に行うことができない者として厚生労働省令で定めるもの
②適正な業務運営を確保するための手順書(GQP、GMP)の整備
申請に係る医薬部外品の品質管理の方法、及び製造販売後安全管理(品質、有効性及び安全性に関する事項
その他適正な使用のために必要な情報の収集、検討及びその結果に基づく必要な措置をいう。以下同じ。)の方法が、
厚生労働省令で定める基準に適合させる必要があります。【薬機法第12条の2】
つまり、厚生労働省令(GQP省令・GVP省令)に基づいて適正な業務運営を確保するために、
マニュアル(手順書)を整備する、ということです。
★GQP省令とは・・・
製造工程等の管理や市場出荷後も品質に係る情報や苦情に対し適切に対応する等の、
製造販売承認書に基づく品質、有効性及び安全性を満たした製品を流通させるためのルールを定めている省令
★GVP省令とは・・・
医薬品等を製造販売後、品質、有効性及び安全性に関する事項その他適正な使用のために必要な情報の収集、
検討及びその結果に基づく必要な措置の方法を定めている省令
③責任者の設置
総括製造販売責任者・安全管理責任者・品質保証責任者を設置する必要があります。
これらの責任者が主導して、上記の手順書に基づいて業務を運営していくことになります。
なお、総括製造販売責任者は、医薬部外品製造販売業許可を取得する営業所にて常勤であることに加え、
下記要件を満たす必要があります。
・医薬部外品の総括製造販売責任者の資格【薬機法施行規則第85条第1項】
1.薬剤師
2.大学またはこれと同等以上の学校で、薬学または化学に関する専門の課程を修了した者
3.高校又はこれと同等以上の学校で、薬学又は化学に関する科目を修得した後、医薬品又は
医薬部外品の品質管理又は製造販売後安全管理に関する業務に3年以上従事した者
▲従事経験とは・・・
医薬部外品の製造販売業許可業者での経験を指し、製造業者での経験等は該当しません。
上記の要件を確認するための資料は、
1.「薬剤師免許証」
2.「取得した単位がわかる資料(学校にて発行できる単位取得証明書等)」
3.「2の資料」+「従事経験証明書」
医薬部外品製造業
クリアすべき許可要件は何?
医薬部外品の製造業許可を取得するために必要な要件は、下記の通りです。
①申請者が欠格要件に該当しないこと
②構造設備等が厚生労働省令で定める基準に適合していること
③責任者(責任技術者)の設置
①申請者が欠格要件に該当しないこと
申請者が、下記のいずれかに該当するときは、許可を与えないことができる。
【薬機法第13条第4項第2号・5条第3号】
イ 第75条第1項の規定により許可を取り消され、取消しの日から3年を経過していない者
ロ 第75条の2第1項の規定により登録を取り消され、取消しの日から3年を経過していない者
ハ 禁錮以上の刑に処せられ、その執行を終わり、又は執行を受けることがなくなった後、3年を経過していない者
ニ イからハまでに該当する者を除くほか、この法律、麻薬及び向精神薬取締法、毒物及び劇物取締法(昭和25年法律第303号)
その他薬事に関する法令で政令で定めるもの又はこれに基づく処分に違反し、その違反行為があつた日から2年を経過していない者
ホ 成年被後見人又は麻薬、大麻、あへん若しくは覚醒剤の中毒者
ヘ 心身の障害により薬局開設者の業務を適正に行うことができない者として厚生労働省令で定めるもの
②構造設備等が厚生労働省令で定める基準に適合していること
医薬部外品の製造所の構造設備の基準は、下記の通りです。
【薬局等構造設備規則(S36厚令2)第12条】
《一般区分の医薬部外品製造業者の製造所の構造設備》
一 当該製造所の製品を製造するのに必要な設備及び器具を備えていること。
二 作業所は、次に定めるところに適合するものであること。
イ 照明及び換気が適切であり、かつ、清潔であること。
ロ 常時居住する場所及び不潔な場所から明確に区別されていること。
ハ 作業を行うのに支障のない面積を有すること。
二 防じん、防虫及び防そのための設備又は構造を有すること。
ホ 床は板張り、コンクリート又はこれに準ずるものであること。
ヘ 廃水及び廃棄物の処理に要する設備又は器具を備えていること。
ト 作業員の消毒のための設備を有すること。
チ 製造品目により有毒ガスを発生させる場合には、その処理に要する設備を有すること。
三 作業所のうち、原料の秤量作業、医薬部外品の調整作業、充てん作業又は閉そく作業を行う作業室は、
次に定めるところに適合するものであること。
イ 作業室内に備える作業台は、作業を円滑かつ適切に行うのに支障のないものであること。
ロ 作業員以外の者の通路とならないように造られていること。ただし、当該作業室の作業員以外の者による
医薬部外品への汚染のおそれがない場合は、この限りでない。
ハ 出入口及び窓は、閉鎖することができるものであること。
ニ 天井は、板張り、コンクリート又はこれらに準ずるものであり、かつ、ごみの落ちるおそれのないように張られていること。
ホ 床は、表面がなめらかですき間のないコンクリート、タイル、モルタル、板張り又はこれらのものと同じ程度に
汚れをとることができるものであること。
ヘ 室内のパイプ、ダクト等の設備は、その表面にごみがたまらないような構造のものであること。
ただし、清掃が容易である場合は、この限りでない。
四 原料、資材及び製品を衛生的にかつ安全に貯蔵するために必要な設備を有すること。
五 製品等及び資材の試験検査に必要な設備及び器具を備えていること。
ただし、当該製造業者等の他の試験検査設備又は他の試験検査機関を利用して自己の責任において
当該試験検査を行う場合であって、支障のないと認められるときは、この限りでない。
《無菌医薬部外品区分製造業者の製造所の構造設備》
一般区分に定めるもののほか、次の通りとすること。
一 作業所は、次に定めるところに適合するものであること。
イ 作業所のうちに作業室又は作業管理区域(作業室及び廊下等から構成されていて、
全体が同程度に清浄の維持ができるように管理される区域をいう。以下に同じ)は、
温度及び湿度を維持管理できる構造及び設備を有すること。
ロ 原料の秤量作業(無菌原薬(無菌である原薬をいう。以下に同じ。)に係る製品の作業所における作業を除く。)
又は容器(無菌原薬に係る製品の作業所においては、滅菌のために行う調製作業以後の作業において用いるもの
に限る。)の洗浄作業を行う作業室は、防じんのため、密閉構造であること。
ニ 無菌原薬に係る製品の作業所のうち、滅菌のために行う調製作業以後の作業の作業室(調製条件によって
菌の増殖を抑制できる場合を除く。)及び無菌医薬品(無菌原薬を除く。)に係る製品の作業所のうち、
薬剤の調製作業、充てん作業又は閉そく作業を行う作業室又は作業管理区域は、次に定めるところに適合するものであること。
イ 天井、壁及び床の表面は、消毒液等による噴霧洗浄に耐えられるものであること。
ロ 設備及び器具は、滅菌又は消毒が可能なものであること。
三 次に掲げる試験検査の設備及び器具を備えていること。
ただし、当該製造業者等の他の試験検査設備又は他の試験検査機関を利用して自己の責任において
当該試験検査を行う場合であって、支障がないと認められるときは、この限りでない。
イ 密閉状態検査を行う必要がある場合には、密閉状態検査の設備及び器具
ロ 遺物検査の設備及び器具
ハ 製品等及び資材の理化学試験の設備及び器具
二 無菌試験の設備及び器具
ホ 発熱性物質試験を行う必要がある場合には、発熱性物質試験の設備及び器具
へ 生物学的試験を行う必要がある場合には、生物学的試験の設備及び器具
《包装等の医薬部外品製造業者の製造所の構造設備》
一 製品等及び資材を衛生的かつ安全に保管するために必要な構造及び設備を有すること。
二 作業を適切に行うのに支障のない面積を有すること。
三 製品等及び資材の試験検査に必要な設備及び器具を備えていること。ただし、当該製造業者の他の試験検査設備
又は他の試験検査機関を利用して自己の責任において当該試験検査を行う場合であって、
支障のないと認められるときは、この限りでない。
③責任者(責任技術者)の設置
医薬部外品製造業者は、厚生労働省令の定めるところにより、医薬部外品の製造を実地に管理させるために、
製造所ごとに、責任技術者を置く必要があります。【薬機法第17条第5項】
責任技術者は、保健衛生上支障を生ずるおそれがないように、その製造所に勤務する従業員を監督し、
製造所の構造設備及び医薬部外品その他の物品を管理し、その他その製造所の業務につき、
必要な注意をしなければなりません。【薬機法第17条第6項で準用する8条第1項】
責任技術者は、医薬部外品製造業許可を取得する製造所にて常勤であることに加え、下記要件を満たす必要があります。
・医薬部外品の責任技術者の資格【施行規則第91条第1項】
1.薬剤師
2.大学等で、薬学または化学に関する専門の課程を修了した者
3.高校又はこれと同等以上の学校で、薬学又は化学に関する科目を修得した後、
医薬品、医薬部外品の製造に関する業務に3年以上従事した者
なお、施行令第20条第2項の規定により厚生労働大臣が指定する医薬部外品(GMP適用有医薬部外品)
を製造する製造所にあっては、責任技術者は薬剤師でなければいけません。
▲従事経験とは・・・
医薬部外品の製造業許可業者での経験を指し、製造販売業者での経験等は該当しません。
上記の要件を確認するための資料は、
1.「薬剤師免許証」
2.「取得した単位がわかる資料(学校にて発行できる単位取得証明書等)」
3.「2の資料」+「従事経験証明書」
許可取得後の手続き
医薬部外品の許可を取得後に必要な主な対応は下記の通りです。
①許可証の掲示【薬機法施行規則第114条による同施行規則第3条準用】
製造販売業・製造業の許可証を、許可を取得している事業所の見やすい場所に掲示しなければなりません。
②GQP省令、GVP省令の遵守(製造販売業者)
手順書に基づき品質管理や製造販売後安全管理に関する業務を行うと共に、記録等を適切に管理する必要があります。
また、改定が必要な場合は、改定日・改定内容・改定理由を記録し、業務の実態に合わせた手順書を整備する必要があります。
③変更等の届出【薬機法第19条第1項及び第2項】
下記事項を変更した場合は、変更事由発生後30日以内に届け出ることが義務付けられています。
1.休止、再開、廃止の場合
2.製造販売業者・製造業者の氏名又は住所の変更
法人の場合は、登記された名称及び住所、個人の場合は、個人の姓名及び住所が変更した場合に、手続きが必要となります。
3.総括製造販売責任者・責任技術者の氏名及び住所の変更
上記責任者が交替になった場合にも、手続きが必要になります。
4.業務委に従事する役員の変更(法人の場合)
5.主たる機能を有する事務所(製造所)の名称及び所在地の変更
許可を取得している(業許可証に記載されている)事務所の名称と所在地が対象になります。
製造所の移転の場合は、同じ都道府県内であっても、新規許可の手続きが必要になります。
製造所の他府県への移転は、移転先の都道府県での新規許可申請が必要です。
6.構造設備の主要部分の変更(製造業者)
製造所の改装に伴う構造設備が大幅に変更した場合や、製造ラインの改廃が該当します。
7.他の種類の許可の新規取得や廃止を行った場合
医薬品・医薬部外品・医療機器等の許可の取得・廃止があった場合、変更届の手続きが必要となります。
④更新申請
製造販売業許可及び製造業許可の有効期限は、許可取得日から5年間です。
事業を継続する場合は、更新手続きが必要となります。
許可更新申請後、新しい許可証が発行されるまでの標準事務処理期間が設定されていますので、
許可有効期限直前ではなく、有効期限の2~3ヶ月前に更新申請書を提出する必要があります。
★更新申請では、新規申請時同様、行政担当官の立入調査があります。その際に、手順書に基づいた記録等が
適切に管理されているかも審査対象になります。記録等が適正に管理できていない場合は、許可を更新できない可能性があります。
⑤医薬部外品製造販売承認
医薬部外品の製造販売業者は、医薬部外品の製造販売をしようとするときには、あらかじめ、品目ごとに、
主たる機能を有する事務所の所在地の都道府県知事に製造販売届書を届け出なければなりません。【薬機法第14条】
つまり、医薬部外品を製造販売するためには、
医薬部外品製造販売業(会社としての許可)と医薬部外品製造販売承認(商品としての承認)が必要になるということです。
また、国外から輸入した医薬部外品を製造販売する際は、外国製造販売業者(製造業者)届書にて、
輸入元となる外国の製造販売業者・製造業者についての情報(製造業者の名称・所在地等)を
PMDA(独立行政法人医薬品医療機器総合機構)経由で厚生労働大臣宛に提出することが義務付けられています。
国内商品の場合・・・「医薬部外品製造販売承認」
国外商品(輸入品)の場合・・・「医薬部外品外国製造販売業者(製造業者)届書」
「医薬部外品製造販売承認」
手続きの流れ
STEP1:ご相談
初回相談は無料です。
まずは、問い合わせフォームからご連絡ください。
STEP2:面談・お申込み
対面・ZOOM・電話にて、詳細をお伺いします。
お伺いした内容にて、お見積りさせていただきます。
金額やサービス内容に納得いただけましたら、ご依頼いただきます。
STEP3:要件の整備・必要書類のご案内
まずは、要件をクリアしていただきます。
クリアできましたら、必要書類(当事務所で作成できない書類)をご案内します。
ご準備いただけ次第、必要書類をお送りください。
STEP4:書類作成・内容確認
頂いた書類・情報をもとに、書類作成させていただきます。
作成が完了次第、内容のご確認をいただきます。
STEP5:当事務所から申請
内容に問題なければ、申請させていただきます。
申請先から追加書類の指示などがあれば、対応致します。
STEP6:許可証の受領
★当事務所へ依頼するメリット★
・要件整備から許可証の受領まで、一括してサポート致します。
・許可取得後のサポートもご要望に応じて対応可能です。